
Rapport – Bilan de la consultation sur l'avenir des essais cliniques
Rapport – Bilan de la consultation sur l'avenir des essais cliniques
Liens connexes
Introduction
Les Instituts de recherche en santé du Canada (IRSC) s'appliquent à renforcer la filière des essais cliniques afin d'améliorer les soins de santé et les résultats cliniques pour toute la population canadienne, et c'est pourquoi ils sont en voie d'établir une stratégie à long terme à cet effet. À l'automne 2022, les IRSC ont lancé une consultation en ligne, intitulée Définir l'avenir des essais cliniques, auprès du milieu de la recherche, des partenaires et des intervenants intéressés par les essais cliniques. Les participants ont été appelés à répondre à des questions sur le rôle des IRSC dans le financement des essais cliniques et dans l'établissement de politiques et de programmes connexes. Les échanges entre les participants, de même que leurs recommandations préliminaires, permettront d'éclairer les discussions continues sur la création d'une stratégie à long terme axée sur les essais cliniques.
Entre le 28 septembre et le 1er décembre 2022, les IRSC ont reçu un total de 44 réponses de la part de chercheurs, de groupes de patients et de citoyens, de réseaux de recherche et de santé, de ministères et d'autres organisations. Elles colligent les commentaires de plus de 140 personnes, qui représentent plus de 100 organisations et groupes d'intervenants.
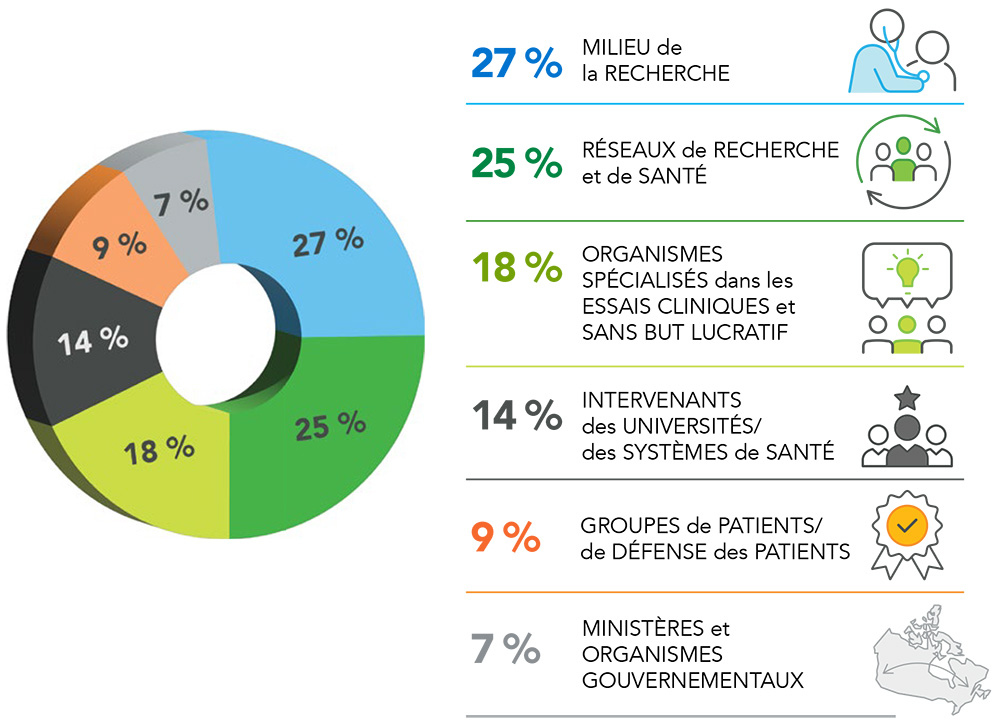
Figure 1. Groupes d'intervenants ayant fourni des commentaires
Description détaillée
Ces 44 réponses colligent les commentaires de plus de 140 personnes, qui représentent plus de 100 organisations et groupes d’intervenants. De ces 44 réponses : 27 % provenaient du milieu de la recherche; 25 %, de réseaux de recherche et de santé; 18 %, d’organismes spécialisés dans les essais cliniques (structures facilitatrices et organisations sans but lucratif comprises); 14 %, d’acteurs du système de santé ou du milieu universitaire; 9 %, de groupes de patients et de défense des intérêts; 7 %, de ministères et d’organismes gouvernementaux.
Points saillants
Les participants ont cerné les principaux obstacles à la réalisation d'essais cliniques au Canada. Ils ont également présenté des solutions novatrices et durables ainsi que les leçons tirées des modèles d'essais cliniques suivis à l'échelle internationale.
-
Obstacles à l'avancement des essais cliniques au Canada
- Duplication des processus, en plus de la complexité des exigences contractuelles et des délais et des ressources déraisonnables s'appliquant au démarrage d'essais cliniques, notamment les lacunes patentes dans l'évaluation de l'éthique de la recherche, dans les procédures d'approbation des établissements et dans les examens réglementaires qui concernent les essais cliniques multicentriques.
- Complexité des processus de demande de financement auprès des IRSC.
- Manque de soutien structurel pour les programmes d'essais cliniques qui se traduit par une délégation des tâches administratives et opérationnelles à des organismes de santé déjà surchargés.
-
Recommandations sur l'amélioration du financement des IRSC à l'appui des essais cliniques
- Créer une structure pancanadienne axée sur la coordination des efforts, la réduction de la duplication et l'intégration des infrastructures existantes (réseaux sur les essais cliniques, unités de soutien de la SRAP, etc.).
- Permettre aux chercheurs et aux unités de soins de santé sans affiliation universitaire d'accéder au financement affecté aux essais cliniques, et assurer la pérennité des infrastructures de financement et de formation associées aux programmes d'essais cliniques afin de favoriser la rétention du personnel hautement qualifié.
- Réserver des fonds à l'ensemble de la filière du développement des médicaments, de la phase de recherche exploratoire aux phases subséquentes aux essais cliniques.
- Uniformiser les exigences administratives relatives à la formation de partenariats avec les patients et accorder des délais suffisants pour leur mise en place, et offrir des orientations et élaborer des directives propices à l'établissement de partenariats entre l'industrie et le milieu universitaire dans l'optique de stimuler l'innovation au Canada.
-
Suggestions concernant l'orientation du financement pour des essais cliniques novateurs
- Intégrer les essais axés sur les plateformes adaptatives, les protocoles de référence (plans flexibles qui permettent une adaptation rapide aux nouvelles connaissances et à l'apparition de traitements potentiels), les essais randomisés par grappes et les études de cohortes qui intègrent la collecte de données en situation réelle.
- Mettre en place un système de données sur la santé qui préserve la confidentialité tout en permettant l'accès à la recherche et l'échange de données.
- Appuyer des essais cliniques décentralisés qui reposent sur des innovations technologiques permettant de recueillir des renseignements à distance en vue d'accroître l'accès aux essais cliniques pour toute la population canadienne.
-
Commentaires sur les priorités relatives aux essais cliniques dans le cadre de la Stratégie en matière de biofabrication et de sciences de la vie du Canada
- Élargir l'admissibilité aux mécanismes de soutien à la recherche préclinique et à la recherche translationnelle, et consacrer des fonds aux essais cliniques précoces (projet pilote, phase 1 et phase 2) dans le but de stimuler la croissance des secteurs du développement de médicaments et de la biofabrication.
- Assurer l'allocation continue et durable de fonds au personnel de recherche clinique essentiel et apporter un soutien au financement d'infrastructures spécialisées, comme des installations à proximité d'établissements de santé pour les essais cliniques de phase 1 et des installations de bonnes pratiques de fabrication au pays.
- Renforcer les capacités du Canada à mettre au point des produits expérimentaux et médicaux au moyen de partenariats entre le milieu universitaire et le secteur privé.
- Offrir aux chercheurs des formations exclusivement centrées sur les essais cliniques, qui abordent des sujets comme les plans d'étude, la biostatistique, les questions éthiques, la confidentialité des données, les processus réglementaires, la sécurisation culturelle, les méthodes de recherche translationnelle ou encore la mobilisation significative des patients et des intervenants.
-
Conseils relatifs aux politiques des IRSC pour favoriser l'équité, la diversité et l'inclusion, la transparence et l'excellence en recherche
- Accroître la diversité des participants aux essais cliniques (enfants, personnes handicapées ou socialement vulnérables, populations en quête d'équité et groupes sous-représentés dans les sciences).
- Recueillir des renseignements sur le profil démographique des personnes qui participent aux essais cliniques, et assurer la transparence des données désagrégées.
- Rendre obligatoires les partenariats avec les patients et faciliter la mise en relation d'équipes menant des essais cliniques avec des organismes qui disposent d'une expertise dans le domaine de la mobilisation de patients (comme la SRAP).
- Stimuler l'innovation au moyen d'essais cliniques décentralisés qui favorisent un accès ouvert et équitable pour diverses populations.
- Établir des critères d'évaluation et des normes portant sur le respect des principes d'équité, de diversité et d'inclusion, et intégrer une section réservée aux résultats significatifs déclarés par les patients dans les demandes de financement d'essais cliniques.
- Élaborer une stratégie de mobilisation des peuples autochtones.
-
Principaux éléments à considérer dans la création d'une stratégie à long terme axée sur les essais cliniques
- Intégrer des essais cliniques au système de santé, et offrir du soutien structurel aux programmes d'essais cliniques et au personnel hautement qualifié.
- Coordonner à l'échelle nationale des activités de création d'essais cliniques (questions éthiques et contractuelles, etc.) et les mécanismes d'échange de données et de transparence de la recherche (formulaires de demande de participation normalisés, lignes directrices minimales relatives au consentement, modèles d'accords, etc.).
- Promouvoir la participation de l'ensemble de la population canadienne à la recherche clinique.
- Faire participer de manière significative des patients à l'établissement des priorités de recherche et à l'élaboration des protocoles d'essais cliniques afin d'assurer la convergence des résultats de recherche avec les attentes des patients.
- Favoriser le leadership des IRSC sur le plan national et international dans le domaine des essais cliniques.
- Établir des programmes de financement à long terme comportant des cycles prévisibles d'appels de demandes de subventions qui permettent la constitution de dossiers solides dans des délais raisonnables.
- Renforcer les capacités du personnel hautement qualifié et apte à mener des essais cliniques au moyen de programmes de formation portant sur la conception d'essais, la biostatistique, la conformité réglementaire, l'assurance de la qualité et l'administration de la recherche clinique.
-
Recommandations sur la prise en compte des pratiques exemplaires d'autres pays
- Le National Institute for Health and Care Research (NIHR) du Royaume-Uni constitue un bon modèle à suivre pour le financement des infrastructures et l'application des connaissances.
- Le modèle mis en place par le National Institutes of Health des États-Unis comporte des composantes dignes d'être reproduites, comme le Planning Grant Program, le National Center for Advancing Translational Sciences, le programme Accelerating Medicines Partnerships et le Patient‑Centered Outcomes Research Institute.
- La priorisation de la recherche doit être un processus continu qui tient compte de considérations diverses et variées, comme les priorités en santé de la population canadienne, l'incidence de la recherche sur le système de santé et la coordination des activités de recherche. La James Lind Alliance du NIHR a été mentionnée à plusieurs reprises pour la pertinence de son modèle.
Prochaines étapes
Les essais cliniques représentent un outil de recherche essentiel pour optimiser la prestation de soins qui exige la coordination des processus scientifiques, cliniques et administratifs, et la prise en compte de divers points de vue. Les commentaires reçus revêtent ainsi une importance cruciale et guideront les futurs échanges visant à cerner les lacunes et à orienter l'élaboration d'une stratégie à long terme en appui à la recherche, à la formation et aux infrastructures à l'égard des essais cliniques réalisés au Canada. Nous tenons à remercier tous les participants de leur apport à la consultation.
Pour obtenir de plus amples renseignements, veuillez écrire à clinicaltrials-essaiscliniques@cihr-irsc.gc.ca.
- Date de modification :